Ионные жидкости на главную
на главную
вещеста, которые при комнатной температуре (и ниже) находятся в жидкой фазе и состоят исключительно из анионов и катионов, называются ионными жидкостями
Повышенная растворяющая способность
В нашей группе была разработана одна из первых теорий ионных жидкостей, которая помимо электростатических учитывает силы Ван-дер-Ваальса между ионами [1-5].
Нам впервые удалось объяснить повышенную растворяющую способность ряда ионных жидкостей по сравнению с неионными [1].
Уменьшение поверхностного натяжения
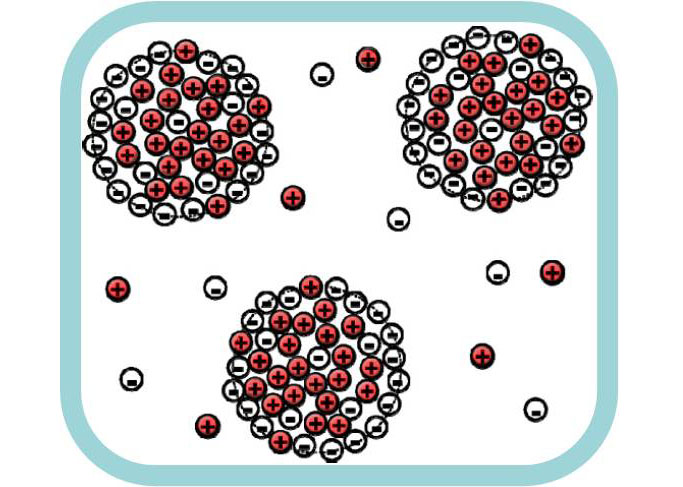
Другим важным предсказанным эффектом, который нашел экспериментальное подтверждение, было уменьшение поверхностного натяжения на границе раздела ионных и неионных жидкостей [2], причем, при определенных условиях, натяжение может становиться отрицательным, что означает неустойчивость макрофазы и образование кластеров ионной и неионной жидкости [3]. Позднее возможность образования кластеров была подтверждена в компьютерных экспериментах.
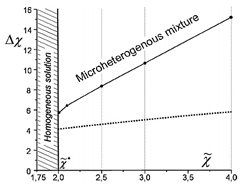
Фазовая диаграмма смеси ионной и неионной жидкостей. Пунктирная линия разделяет микроскопическую и макроскопическую фазы